来源:宝创日期:2026-04-30(9)
近日,美国两项具有广泛影响力的宫颈癌筛查指南相继更新,正式将HPV自采样检测纳入推荐,为广大女性提供更便捷、更私密的筛查选择。

美国癌症协会(ACS)在最新发布的宫颈癌筛查指南中明确指出,女性可通过自行采集样本(自采样)的方式进行人乳头瘤病毒(HPV)检测。此次指南的更新扩展了2020年ACS针对平均风险妇女的宫颈癌筛查建议,意味着居家筛查不再只是“备选”,而是被正式写入权威指南的可靠方式。
指南建议:
l首选临床医生采样的方式进行HPV初筛,阴性结果的女性每5年进行1次的重复筛查;
l对于25–65岁平均风险的女性,可选择阴道自采样作为HPV检测的方式,阴性结果的女性建议在3年后进行重复筛查;
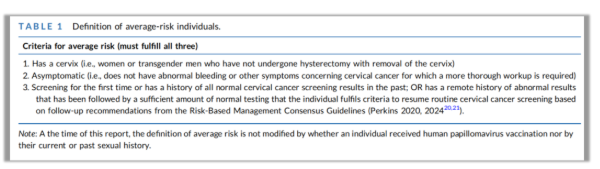
表1 平均风险个体的定义
多项研究证实,基于PCR方法进行HPV自采样与临床医生采样,两者在检测高危型HPV感染和宫颈癌前病变的灵敏度及特异性相当。这些证据证实了自采样用于HPV检测的临床有效性和可靠性,并支持将其纳入宫颈癌筛查指南。
目前,FDA已批准HPV自采样作为一种安全可靠的宫颈癌筛查方式,为适龄女性的筛查提供了新选择。
2026年1月,美国卫生资源与服务管理局(HRSA)也在其宫颈癌筛查指南中加入了自采样的推荐:首次将女性自行采集样本(自采样)进行HPV检测的方式列为推荐建议,并于权威期刊《美国医学会杂志》(JAMA)发表。
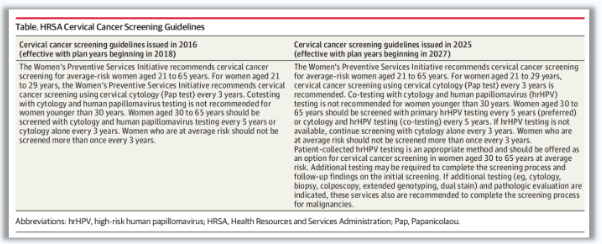
表2 HRSA指南更新内容
值得注意的是,HRSA的此次更新还带来了关键性政策保障:自2027年1月1日起,保险将覆盖符合条件女性的HPV自采样费用(包括后续的检测费用)。
本次指南更新将有助于提高宫颈癌筛查的可及性,特别是为农村地区居民、行动不便者以及医疗资源获取困难的人群,提供一个更便捷、更具隐私性的筛查选择,这意味着女性无需再亲自前往医院,通过样本寄送的方式即可完成HPV检测,真正实现“足不出户,完成筛查”。
宝创生物现已推出HPV系列自采样盒套装,广大适龄女性无需再前往医院排队挂号候诊采样,在家即可自行轻松完成样本采集,寄回后即可获取专业检测报告,让您的宫颈健康监测更私密、更便捷、更可及。
涵盖国家卫健委要求检测的14种高危型别,聚焦HPV致癌基因的表达,不只关注病毒,更锁定病变风险,有效鉴别持续性感染,助力宫颈病变早期预警。
全面覆盖31种HPV型别(14种高危型+4种中危型+13种低危型),不仅适用于宫颈癌防控,还可预警皮肤疣、生殖器相关疾病,助力多维度健康管理。